Methanhydrat - das brennende Eis
Ein faszinierender Stoff wird erforscht
von Prof. Dr. Tina Treude
Nordostpazifik, hundert Kilometer vor der Küste des US-Bundesstaates Oregon. Das deutsche Forschungsschiff SONNE liegt ruhig im Wasser. Frauen und Männer in Arbeitsoveralls oder in Ölzeug stehen an der Reling und beobachten die Wasseroberfläche. Andere konzentrieren sich auf mehrere Bildschirme an Deck. Vor eine halben Stunde haben sie den Videogreifer, eine Art High-Tech-Baggerschaufel mit Kameras, in die Tiefe gelassen. 800 Meter unter dem Schiff erstreckt sich der sogenannte „Hydratrücken“, eine der bekanntesten Lagerstätten für Methanhydrate. Von dort unten soll der Greifer Proben holen. Mittlerweile hängt er knapp über dem Meeresboden. Gespannt verfolgen die Wissenschaftler die Bilder, die die Kameras zu den Bildschirmen an Deck schicken. Als ein vielversprechendes Stück Meeresboden ins Blickfeld gerät, lassen die Forscher die Backen des Greifers im Sediment zuschnappen. Meter für Meter holt die Winde der SONNE das Stahlseil mit dem Greifer wieder ein. Die Spannung steigt: Hat sich die Probenentnahme wirklich gelohnt? Nach einer weiteren halben Stunde durchbricht das schwere Gerät die Wasseroberfläche und schwingt über das Arbeitsdeck des Schiffes. Die Backen öffnen sich und entlassen einen Haufen Schlamm. Tatsächlich: Zwischen dem dunklen Sediment schimmern weiße Brocken hervor – Methanhydrat. Die Spannung der vergangenen Stunde löst sich. Jetzt heißt es schnell arbeiten. Die Frauen und Männer stürzen sich auf den Haufen, legen mit Schaufeln die weißen Brocken frei und säubern sie vom Schlamm. Mit geübten Handgriffen setzen sie Bohrer an und entnehmen Proben, die schnell in dampfenden Behältern verschwinden. Diese enthalten flüssigen Stickstoff, minus 194 Grad Celsius kalt. So werden die Proben vor der Zersetzung bewahrt, damit sie später in Laboren an Land genauer analysiert werden können. Alltag auf einer Methanhydratexpedition.
Eine chemische Kuriosität?
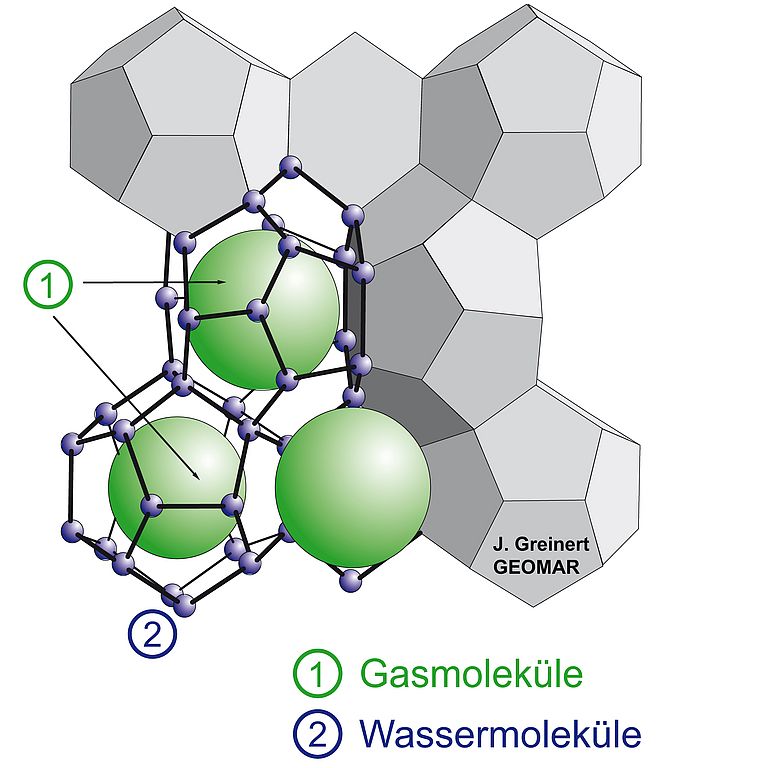
Methanhydrat – was ist das eigentlich? Stark vereinfacht könnte man sagen: Eis mit Erdgas. Oder genauer: Erstarrtes Wasser, dessen Moleküle kristalline Formen bilden – ähnlich wie gewöhnliches Eis. Doch bei den Methanhydraten bilden die Wassermoleküle richtige Käfige, in denen zusätzlich Methanmoleküle gefangen sind. Für das menschliche Auge sieht Methanhydrat trotzdem aus wie normales Eis. Doch wenn es schmilzt, ist Vorsicht angebracht. Denn das entweichende Methan ist dem üblichen Erdgas sehr ähnlich und leicht brennbar. Den Spitznamen „brennendes Eis“ hat das Methanhydrat also verdient.
Damit das Wasser die entsprechenden Formen annehmen und Methan einschließen kann, sind vor allem zwei Bedingungen notwendig: Niedrige Temperaturen und ein hoher Druck. In den Tiefen der Meeren mit einer Temperatur zwischen zwei und vier Grad Celsius muss der Druck ungefähr 50 bar betragen – das entspricht einer Wassertiefe von 500 Metern. Steigt die Temperatur, muss auch der Druck höher werden, damit sich Methanhydrat bilden kann beziehungsweise sich nicht auflöst. Dass sich unter diesen Bedingungen „brennendes Eis“ bilden kann, wissen Forscher schon seit dem frühen 19. Jahrhundert. Allerdings hielten sie es lange für eine chemische Kuriosität ohne Bedeutung. Erst im frühen 20. Jahrhundert erregte Methanhydrat erstmals größeres Aufsehen. Damals begannen Energieversorger, Erdgas durch Pipelines zu pumpen. Das Gas war oft mit Wasser vermischt. Da Gas in Pipelines unter hohem Druck steht, bildeten sich Hydrate, die die Leitungen verstopften. Die Pipelinebetreiber lösten das Problem, indem sie dem Gas vor dem Transport Feuchtigkeit entzogen.
Entdeckung im Pazifik
In den 1970er Jahren schließlich sagten russische Wissenschaftler voraus, dass Gashydrate nicht nur im Labor oder in Pipelines, sondern auch in der Natur in großen Mengen vorkommen müssten – und zwar vor allem in der Tiefsee. Denn dort herrschen gewöhnlich Temperaturen von zwei bis vier Grad Celsius und der Druck ist extrem hoch. Vereinzelte Bohrungen und Funde bestätigten die These. 1996 entdeckte ein Team deutscher Wissenschaftler unter der Leitung des Kieler Professors Erwin Suess schließlich erstmals große natürliche Methanhydratvorkommen vor der Küste Oregons – in genau jener Region, die heute unter Wissenschaftlern als „Hydratrücken“ bekannt ist. Mittlerweile weiß man: Methanhydrate existieren in allen Ozeanen in gigantischen Mengen. Da hoher Druck die Bildung der Hydrate begünstigt, könnte man meinen, dass mit zunehmender Tiefe auch die Menge der Hydrate zunimmt. Das stimmt so allerdings nicht. Denn Methan entsteht im Meer vor allem, wenn Kleinstlebewesen abgestorbenes organisches Material abbauen, das aus den obersten Wasserschichten langsam auf den Meeresboden rieselt. Unterhalb von 2.000 bis 3.000 Metern Tiefe kommt aber kaum etwas von diesem Material an – deshalb fehlt auf den tiefer gelegenen Ozeanböden das Methan. Die idealsten Bedingungen für Methanhydrate findet man an den sogenannten Kontinentalhängen, wo die Kontinentalsockel in die Tiefseeebenen übergehen, in Wassertiefen zwischen 500 und 2.000 Metern. In sehr kalten Regionen, wie zum Beispiel der Arktis, bilden sich Methanhydrate allerdings auch in Wassertiefen um die 200 bis 300 Meter oder im Permafrostboden an Land.
Warum Gashydratforschung?
Biologen, Geologen, Geophysiker und Chemiker – für sie alle sind Gashydrate ein hochinteressantes Forschungsgebiet. Denn auch wenn wir schon einiges über die Verbreitung der Hydrate wissen, sind viele Fragen noch offen. Unter anderem ist noch nicht endgültig geklärt, wie sich Gashydrate genau bilden, unter welchen Bedingungen sie sich zersetzen und in welchem Maß Methan dabei ins Wasser und schließlich in die Atmosphäre abgegeben wird. Wenig bekannt ist auch über die genaue Struktur der Lagerstätten und ihre Verteilung im Meeresboden: Einige liegen knapp unter dem Meeresboden, andere mehrere hundert Meter darunter. All diese Untersuchungen sind Gegenstand der Grundlagenforschung, mit der Forscher versuchen, das System „Methanhydrate“ zu verstehen. Eine andere Frage, an der viele Forscher arbeiten ist, was mit den Hydraten geschieht, wenn die Ozeane wärmer werden. Da die Stabilität der Hydrate von Druck und Temperatur abhängt, könnten sie sich bei steigenden Temperaturen auflösen. Das wiederum hätte möglicherweise katastrophale Folgen. Denn die Hydrate stabilisieren die Kontinentalhänge, an denen sie vorkommen, wie eine Art Zement. Lösen sie sich auf, kann dies zu Hangrutschungen führen. Die Rutschung erzeugt eine Einwölbung der Meeresoberfläche, welche beim Zurückschnellen eine Welle in Gang setzt, die sich über flachem Wasser zu einer gigantischen Flutwelle – einem Tsunami – aufbäumen und ganze Küstenstreifen verwüsten kann. Es gibt Untersuchungen, die vermuten lassen, dass sich eine solche Katastrophe vor 8.000 Jahren vor der Küste Norwegens abgespielt hat. Nicht auszudenken, welche verheerende Folgen solch ein Tsunami bei der dichten Küstenbesiedlung heutzutage in Nordeuropa anrichten hätte.
Methan als Klimagas
Doch Tsunamis sind nicht die einzige Sorge, die uns Methanhydrate bereiten sollten. Methan ist ein starkes Treibhausgas. Seine Eigenschaft als solches ist etwa 23 Mal stärker als die des Kohlendioxides. Eine Auflösung großer Mengen Gashydrate könnte somit den Treibhauseffekt deutlich beschleunigen. Indizien deuten darauf hin, dass eine enorme Freisetzung von Methangas bereits vor 55 Millionen Jahren einen Klimawandel hervorgerufen hat – also kein rein theoretisches Szenario.
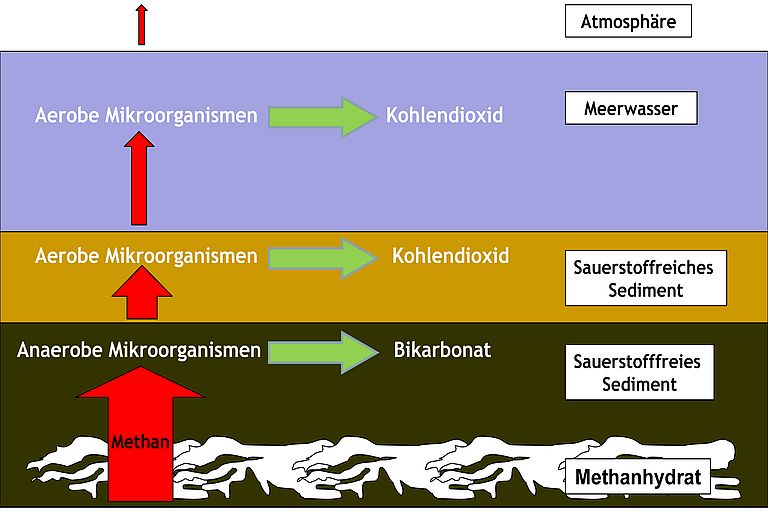
Allerdings würde wohl nicht das gesamte Methan ins Wasser und von dort gleich in die Luft gelangen. Die bisherigen Forschungen zeigen, dass ein Konsortium aus Mikroorganismen im Meeresboden in der Lage ist, bereits einen Großteil des gelösten Methans zu unschädlichem Bikarbonat zu verarbeiten, bevor es ins Wasser gelangt. Im Wasser selbst gibt es wiederum andere Mikroorganismen, welche mit Hilfe von Sauerstoff am Methan knabbern und es in Kohlendioxid umwandeln. Das gilt aber nur bei den Methanmengen, die schon heute natürlich frei im Meeresboden sind. Ob und wie diese Bakterien mit einer massenweisen Auflösung des Hydrats fertig werden würden, ist unklar. Zudem könnten die im Wasser lebenden Methanfresser zu einer Verringerung des Sauerstoffes und einer Erniedrigung des pH Wertes in betroffenen Meeresgebieten führen – Bedingungen, welche einigen Meeresbewohnern Probleme bereiten können.
Methanhydrate als Energielieferant
Seit bekannt ist, dass in den Ozeanen ein gigantischer Vorrat an Methanhydraten lagert, ist das brennende Eis außerdem nicht mehr nur im Fokus einzelner Wissenschaftler, sondern auch von Regierungen und Energiekonzernen. Schließlich ist Methan ein begehrter Energieträger. Aktuelle Schätzungen besagen, dass die Menge an fossilem Brennstoff, der durch Methanhydrate potentiell zur Verfügung stände, bei weitem jene von Erdöl, Kohle und klassisch gefördertem Erdgas übersteigt. Die Zahlen schwanken jedoch, denn zur Berechnung der Methanhydratvolumen gibt es verschiedene Modelle. So finden sich Zahlen zwischen 100 und 530.000 Gigatonnen Kohlenstoff. Zum Vergleich: Die noch existierenden Vorräte der fossilen Brennstoffe Erdöl und Kohle werden auf etwas 5.000 Gigatonnen geschätzt. Allerdings wäre nur ein sehr geringer Teil der Gashydrate tatsächlich als Energiequelle nutzbar, da viele Lagerstätten unerreichbar oder technisch unpraktikabel für den Abbau sind. Auch dabei ist Augenmaß gefragt, um beim Abbau keine ungewollten Nebenwirkungen wie Tsunamis oder die Freisetzung von Methan zu verursachen.
Wir stehen heute erst am Anfang, die komplexen Systeme, welche mit marinen Gashydratvorkommen gekoppelt sind, zu verstehen. Der Großteil der Gashydratvorkommen befinden sich weit unterhalb der Meeresoberfläche und sind nur mit Bohrungen von Plattformen und Tiefseebohrschiffen zu erreichen. Je tiefer man geht, desto größer wird der technische Aufwand. Und mit jeder neuen Entdeckung stößt man auf neue Fragen.
Prof. Dr. Tina Treude ist Meeresbiologin und Biogeochemikerin an der University of California in Los Angeles im Department Atmospheric & Ocean Sciences. Sie arbeitete bis 2014 in der Forschungseinheit "Marine Geosysteme" am GEOMAR Helmholtz-Zentrum für Ozeanforschung Kiel und war Mitglied im Kieler Exzellenz-Cluster "Ozean der Zukunft". Ihr Spezailgebiet ist die Untersuchung von biogeochemischen Prozessen im Meeresboden. Dazu gehört auch die Erforschung von Methan in der Tiefsee.